金屬腐蝕簡介
腐蝕系列檔案:1. 腐蝕測試.SOP 2. 腐蝕試片 3. 腐蝕照片
資料來源:http://210.60.224.4/ct/content/1974/00060054/0010.htm
#作者:劉曉嶺 高嘉鴻 通信處:成功大學 大綱 TOP BOTTOM
總彙系列:1.CNS/EER/積垢/熱傳熱力綜合系列、2.CNS/EER系列/應用、3.總彙.水處理化工技術、4.總彙.水處理術語、5.EER工程.文章總彙、6.E平台-水處理技術
水處理技術系列:1.空調水質污染計算、2.EER問題與改善方法.原理、3.化工技術解說(1)、4.化工技術解說(2)、5.空調技師-水處理設計技術、6.水處理.實用技術及市場狀況
CNS系列檔案:CNS、AHRI技術、CNS、AHRI技術要點、EER節能技術90%、空調主機EER量測驗析實務技術、EER全年確效技術、冰機EER.基準值技術及運用SOP
EER與積垢浪費檔案:EER訪測.中技社、綠基會實測、費用展開表、LCC 20年比較表、積垢與LMTD公式演算
工程效益系列:費用展開表、工程經濟效益評比、偷工減料、損害業主權益
EER改善成效檢驗系列:懶人包(0)、(1)、(2)、穩態EER技術(1)、(2)
成效驗析實務系列:EER驗證分析實務(1)、(2)、EER驗證分析系統畫面
趨近溫度系列:趨近溫度的謬思(1)、(2)、(3)原來一直都錯了、(4)謬思的實證
防蝕效益系列:1. 冷卻水處理腐蝕率標準、2. 水處理防蝕經濟效益技術
法令系列:1水處理採購與法令、2水處理與能源管理法、3水處理與技師法、4.EER工程帶動空調產業發展、5.ESCO產業發展的契機、6水處理與偽造文書、7承商水處理技術
業主系列:1主機EER改善.第一步、2業主進階技術、3基本功、4.CUS/EUS發包範例.解說、5業主再進階技術、6運轉EER改善專案、7精明購買家.知識經濟、8水處理送審範例解說
監造系列:搶標下.業主監造技術(1)、(2)、(3)
腐蝕的電化學 腐蝕的形態 極化
極化與腐蝕速率的關係 陰極保護法 金屬的鈍化
如果和含有氯離子的溶液保持接觸,既使是不銹鋼,也會發生穿孔的腐蝕現象。
話說醬油工廠,運送醬油的輸送管經過水蒸汽日積月累的侵蝕,管子的表皮便因氧化而生成一層層的鐵銹。不僅有礙觀瞻而且也實在破得不能再用了。為了一勞永逸老板只好不惜成本,換裝一套閃閃發光的不銹鋼的輸送管,的確漂亮極了。但遺憾的是好景不長,一星期後,這套仍然發亮的管子居然破了許多小洞,一滴滴的醬油由小洞流了出來。老板大驚,他老兄不禁自言自語地叨唸起來:「這年頭可真怪?不銹鋼怎么會生銹呢?」
老高一百塊錢買的老爺鐵馬,除了車鈴鐺不響,整個車子都可當作樂器用,更糟的是長滿銹的車子,女朋友怎么坐呢?老高心想:「明天又是週末,正是郊遊的好時光,應該把那老爺車好好的整容一番,也好騎車帶心上人去遊山玩水。」說幹就幹,這可真累壞了老高。正當他拖著疲憊的身體面對油亮亮的車子自鳴得意的時候,老友蔡兄卻翩然蒞臨,眼見塗滿油的腳踏車大呼道:「擦車不上油也罷,因為愈上愈容易生銹!」老高聽了不禁愕然。
談到金屬的腐蝕,我們必須考慮其所在之環境。在一般大氣下不銹鋼確是不生銹,但是在含有氯離子的溶液中,不銹鋼就會發生穿孔的腐蝕現象,術語叫做孔蝕(pitting)。醬油工廠以不銹鋼製成的輸送管有孔蝕的現象,就是因為醬油中有氯離子存在的緣故。再說,腳踏車塗油,固然是為了防銹,而我們一般所用的擦車油都是酸性的礦物油。在酸性的溶液中易於腐蝕,正如我們將鐵片投入鹽酸溶液,即發生下列的化學反應:
陽極反應(氧化) Fe→Fe+++2e- 大綱 TOP BOTTOM
陰極反應(還原) 2H++2e-→H2
陽極與陰極的反應構成一個電池。事實上我們也可以在鐵片上看見一粒粒的氣泡,那就是氫氣。
腐蝕的電化學
金屬的腐蝕主要是由於有陽極(anode)及陰極(cathode)的反應而構成一個電池(cell)。金屬的腐蝕反應有下列三種基本形式的電池。
(1)異極電池(dissimilar electrode cell):是由兩種不同的電極所構成的。就如同上述把鐵片投入鹽酸溶液就有氧化還原反應,氧化的電極是鐵電極,還原的電極是氫電極。一般可用的金屬為了特殊目的都含有合金元素。這種合金元素和其母體(matrix)在適當的電解液中即可構成異極電池,而有氧化還原反應,發生氧化反應的電極,就造成金屬的腐蝕。
(2)濃差電池(concentration cell):電池的兩極是相同的金屬,但放在兩極不同的電解液中,使參與反應的離子或反應氣體的濃度不同,這樣所構成的電池稱為濃差電池。濃差電池的第一種形式為鹽性濃差電池(salt concentration cell),(如圖1)所示。左邊的銅放在稀硫酸溶液中,右邊的銅放在濃硫酸溶液中,於是銅離子在右邊的溶液為數較多。根據涅恩斯特方程式(Nernst eguation),左邊的銅就成為陽極(註一),而兩電極的電位差與兩邊銅離子的濃度比的對數成正比: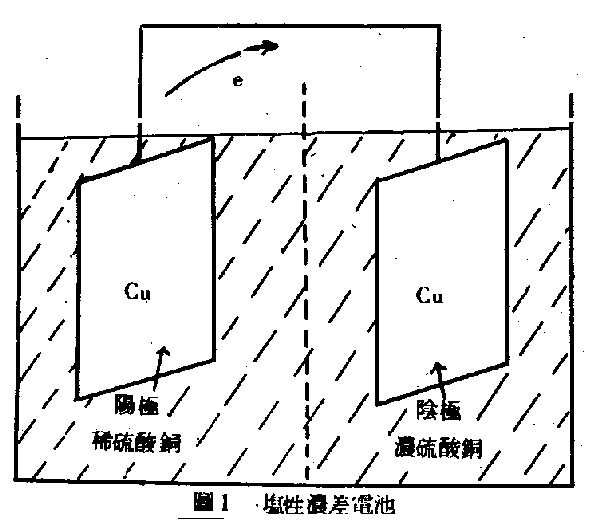
另一種形態的濃差電池為氧濃差電池(differential aeration cell)可用以解釋金屬的吃水線腐蝕(waterline corrosion),即金屬在電解液表面時的腐蝕為最嚴重。
(3)溫差電池(differential temperature cells):電池的兩極相同,但兩極的溫度卻不一致。溫度的高低為陽極或陰極,因金屬的種類而異。以銅為例;高溫者為陰極,低溫者為陽極。但是銀,則剛好相反。
事實上,金屬的腐蝕反應可能為上述三種電池的組合。
腐蝕的形態
腐蝕不僅使金屬生成氧化物造成金屬本身的損失,也可以減低金屬的強度、韌性或生裂痕(cracking),造成金屬材料的破壞。雖然金屬本身的損失不重,但其影響卻很大。這種影響和腐蝕的形態有很大的關係。譬如前述醬油工廠的輸送管如為均勻腐蝕則損失較小,若為孔蝕則損失較大。但對於汽車的軸承,孔蝕損失較小,而均勻腐蝕損失較大。由此可見,腐蝕的形態是很重要的。腐蝕的形態可分為下列五種。
(1)均勻腐蝕(uniform attack)──將鋅電極及氫電極短路(short circuit)置於酸性溶液(如圖2),鋅即發生腐蝕現象。如果把鋅塊投入酸性溶液,鋅照樣會腐蝕(如圖3)。這時在鋅塊的某些部分是局部陽極(local anode),某些部分是局部陰極(local cathode)而構成一局部電地(local cell)。但這些局部陰極和局部陽極會隨時間而改變其位置。因此鋅塊的腐蝕是均勻的。
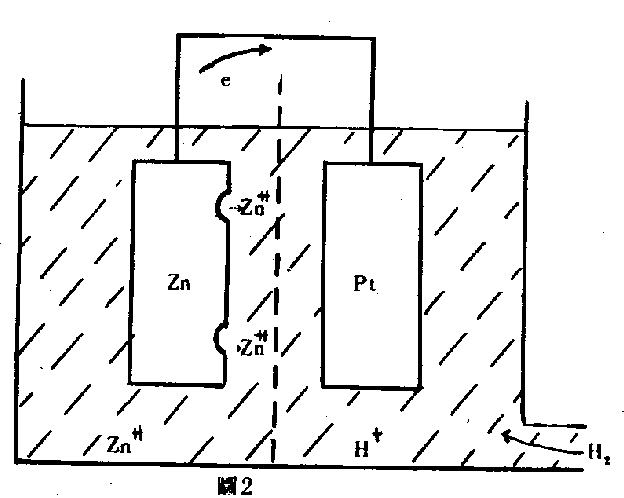
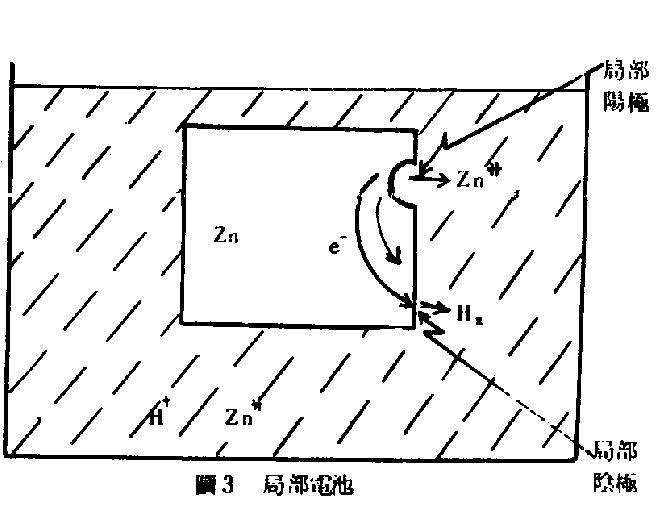
(2)孔蝕(pitting)──此種形態的腐蝕決定於陽極和陰極的面積比。若陽極的位置不隨時間而變化,且陽極的面積遠小於陰極,則陽極的電流密度(currentdensity註二)甚大,因此腐蝕速率較快而產生孔蝕(如圖4)。
陽極反應 Fe→Fe+++2e-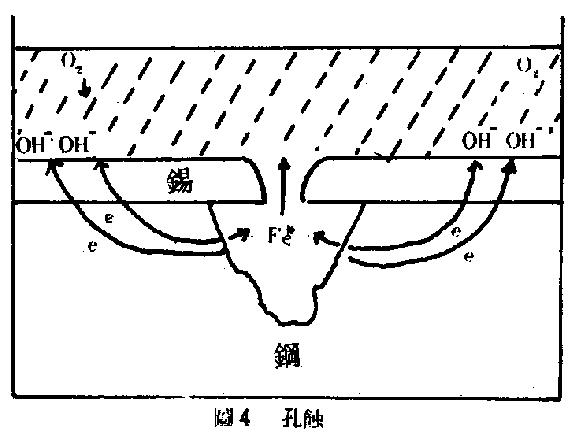
陰極反應 O2+2H2O+4e-→4OH- 大綱 TOP BOTTOM
(3)晶粒間腐蝕(intergranular corrosion)──當一金屬在晶粒界(grain boundary)的化學成分和其晶粒(grain)相差很大時,可能就有這種腐蝕現象發生。例如不銹鋼加熱至500~800℃時,有Cr23C6在晶界析出而降低晶粒中Cr的含量,可能就有這種腐蝕現象。
(4)選擇性腐蝕(selective leaching, parting)──此種腐蝕為固相溶液合金(solid-solution alloy)中之某種元素被侵蝕。例如:黃銅(銅鋅合金)在酸性溶液中的鋅受到腐蝕,而生成鋅的腐蝕物及未被腐蝕的銅。此種形態的腐蝕可應用於金屬特別是貴重金屬的精煉(refining)。
(5)應力腐蝕(stress corrosion):當金屬在某種特殊的環境中受一定張應力(註三)作用,則金屬材料產生裂痕(註四)。
極化
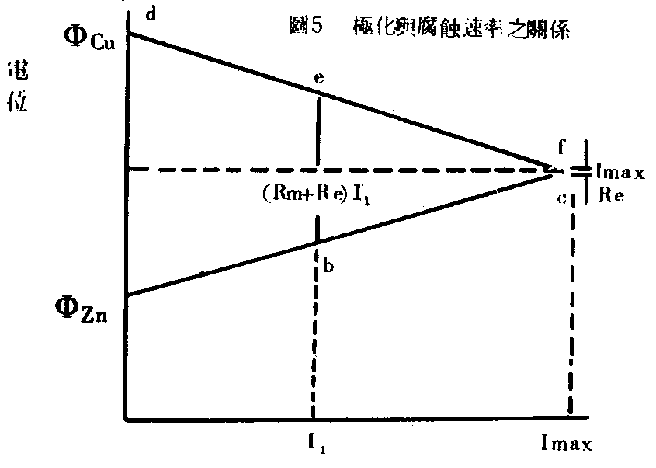
若電極上有電流,則電極與電解液間便不再是平衡。同時電極電位(electrode potential)也隨之改變。而此電位的變動方向總是和電流相反,也就是趨向於消除改變平衡的因素。所以陽極電位總是變為較陰極性的電位,而陰極朝相反方向變動。換句話說,就是陽極電位上升而陰極電位下降。因此兩極的電位差便逐漸減小。電位和電流間的關係(如圖5)所示,這是由於電流通過電極而產生的電位改變,便叫做極化。
(1)濃差極化(concentration polarization)
前面我們已經談過,濃差電池是由於極板在不同濃度的電解液中而有電位差。同理,如果極板近圍的電解液中離子濃度有了變動,極板的電位也隨之而變。例如:銅在硫酸銅溶液中當做陰極時,當電流接上後便有銅在銅板上析出,而使極板附近的銅離子濃度減低。由涅恩斯特方程式知電位隨濃度降低而下降。其減少的量就是銅極上的濃差極化。相對地在陽極上因溶解而提高離子濃度從而電位隨之升高而生極化。若電流加大,則離子濃度增減亦大,極化也就愈大。
(2)活性極化
活性極化乃因電極反應的進行緩慢,換句話說就是反應的進行必須有足夠的活化能(activation energy)來克服能障(energy barrier)的瓶頸。這種瓶頸如發生於陽極上,則陽極反應也會受到抑止。電化學上最常見的氫過電壓(hydrogen overvoltage)就是個最好的例子。氫在陰極上還原,而生成氣泡,其極化就是所謂氫過電壓。在陽極上常有OH-之氧化發生而生成氧氣。
這種陽極極化便稱為氧過電壓(oxygen overvoltage)。
(3)電阻電位降
當電流通過電解液或金屬反應生成物的薄膜(metalreaction product film)時,皆須克服其電阻而有電位降,這種電位降即電流I和電阻R之積,只要有電流必有IR電位降。
極化與腐蝕速率的關係 大綱 TOP BOTTOM
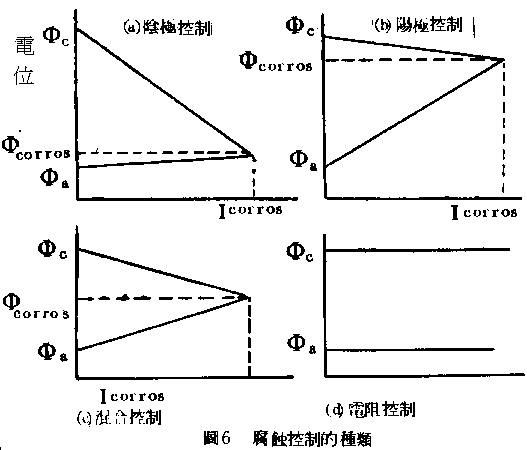
現在就以圖5來討論極化和腐蝕速率的關係,(如圖6)各為銅極和鋅極的敞路電位(open-circuitpotential)。予短路後外電路之電阻漸減,則電流漸增,兩極的電位各沿abc,def線變動,當電流為I1時兩極的電位各為b點及e點所示。此時銅極的極化為e-d,鋅極的極化為b-a,兩極的電位差則為e-b,其值相當於I1(Rm+Re)。其中Rm為外電阻,Re為電解液之電阻。當外電阻趨近於零,此時電流為最大(Imax)。電位差即電流通過電解液之電位降ImaxRe。Imax亦稱腐蝕電流,因腐蝕速率與Imax有正比關係。由圖可知,若極化增大則abc,def的斜率絕對值增大,而Imax(或Icorros)減小,腐蝕速率亦小。在金屬面上的局部電池上,因陽極和陰極很接近,所以電解液的電位降幾乎不具影響。而兩極板上之極化成為主要的決定速率因素。若陽極上的極化遠比陰極為大時,則陽極反應之抵抗大於陰極而成為速率決定階段。此時之腐蝕反應稱為陽極控制(anodic control),其情形如圖6(b)所示。相反地,如果陰極極化遠大於陽極便成為陰極控制(cathodic control)圖6(a)。通常兩極上各有相當程度的極化,這種情況稱為混合控制(mixed control)圖6(c)。還有一種電阻控制(resistance control)圖6(d)這種情形是在電解液或生成物具有高電阻時才存在,因高電阻之下的電流太小,不足引起大量極化,使得電阻成為控制速率因素。通常我們在金屬上塗一層絕緣物(如油漆)便是利用其高電阻降,低電流密度以防腐蝕的。
陰極保護法 大綱 TOP BOTTOM
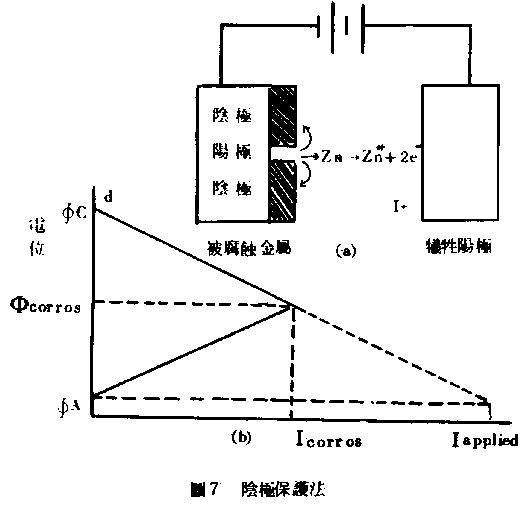
陰極保護便是利用極化的原理,以保護金屬最好的例子。我們知道腐蝕的進行必然伴隨電流,如果設法阻止這種電流,或者設法消除金屬面上的電位差,便可防止腐蝕。陰極保護就是準此原則設法加大陰極的極化,使其電位降到和陽極相等。其方法是加個外電以使陰極電位下降如圖7(a)。其極化如圖7(b),金屬面上的陰極和陽極在未施陰極保護時其腐蝕電流為Icorros。加上外電流後陰極的極化增加,電位降低。當陰極的電位降到和陽極相等時,陰極上的電流為Iapplied,而被腐蝕金屬在陽極上因為沒有電流故而受到完全的保護。
若一金屬具有很大的腐蝕傾向,但其腐蝕速率卻很小,此種現象稱為鈍化。鈍化的發生乃是因為金屬表面生成鈍化膜(passive films),其厚度甚薄僅有20A。這層膜具有雙重作用;第一它本身不會生長,第二它能阻止金屬氧化。不銹鋼在一般環境中不生銹就是因為形成鈍化之故。通常有兩種理論可解釋鈍化現象:
(1)氧化膜理論(oxide film theory)──根據這理論,鈍化膜就是一種氧化膜,它是腐蝕生成物,而成為氧氣擴散的阻礙,因而隔絕金屬及其環境達到防蝕的目的。
(2)吸附理論(adsorption theory)──金屬成為鈍化的原因為其表面吸附氧原子形成鈍化膜。根據這個理論,金屬元素的d軌道一定要有空間方能吸附氧原子。
金屬中加入能形成鈍化的合金元素,則其腐蝕速率減小,但是含有鹵素離子──特別是氯離子──的環境則具有破壞鈍化膜的作用,因為氯離子對於氧化膜具有很強的穿透性(氧化膜理論)或者說氯離子較O2,OH-更易吸附於金屬表面(吸附理論)。氯離子破壞鈍化膜是選擇在膜的最薄或是具有缺陷(defect)的地方。在膜破處的金屬為陽極,而其他未被破壞之處則為陰極,形成鈍性一活性電池(passive-active cell)。因陽極的面積甚小且不隨時間而改變其位置,故有孔蝕的現象。但如非鈍化金屬,便沒有這種現象。
上面我們已經談了一些有關金屬腐蝕的基本知識,讀者若意猶未盡,可參考下列各書:
(1)Uhlig著「Corrosion and Corrosion control」本文依據之藍本。
(2)陸志鴻著「金屬物理學」正中書局,第十二章。
(3)Van Vleck著「Elements of Material Science」第十二章。
(4)Guy著「Iutroduction to Mateial Science」
註一:本文所用的電位均為還原電位。
註二:電流密度為單位面積(陽極或陰極)所通過之電流。
註三:此處所指的應力除了外力外,尚有因冷作加工,熱處理等存於金屬內的應力。
註四:關於應力腐蝕,科學月刊第二卷第八期(總號第二十期)「金屬應力蝕裂」一文中有詳盡介紹。
如果您有其他見解或心得,歡迎您到FB陳新湧、運轉EER技術論壇、新湧產業論壇發表
如果您有任何疑問,歡迎您聯絡新湧或email告知,讓我們為您服務。









